Kameras für Fluoreszenzmikroskopie
Fluoreszenzmikroskopie ist eine übergreifende Technologie, die zahlreiche Felder abdeckt. Das reicht von grundlegenden Anwendungen in den Biowissenschaften bis hin zu hochentwickelten Techniken, bei denen nur sehr wenige Photonen oder einzelne Moleküle durch spezifische High-End-Hard- und Software erkannt und lokalisiert werden.

Bei der Wahl einer Kamera für die Fluoreszenzmikroskopie muss ein Gleichgewicht zwischen bestimmten Sensoreigenschaften, kamerabezogenen Themen und den Bedürfnissen der beabsichtigten Anwendungen in Wissenschaft, Medizin oder Industrie gefunden werden.
Optisches Format und Auflösung
Betrachtet man den sichtbaren Wellenlängenbereich, so unterscheiden sich die Überlegungen zum optischen Aufbau hinsichtlich Format, Vergrößerung und Auflösung nicht wesentlich von normalen Lichtmikroskopie-Anwendungen. Es ist jedoch wichtig zu wissen, dass die Gesamtkosten steigen, wenn größere optische Formate wie der F-Mount verwendet werden. Am gebräuchlichsten ist der C-Mount, der eine sehr gute optische Leistung bietet und für den die meisten Produkte und Lösungen zu einem vernünftigen Preis erhältlich sind. Der kleinere S-Mount ist eine gute Wahl, wenn größenbeschränkte und preisgünstige Instrumente entwickelt werden. Quadratische Sensoren werden oftmals bevorzugt, um den maximalen Bildinhalt zu erfassen.
Da der Sensor eine zentrale Rolle in einem bildgebenden System übernimmt, ist die Auswahl hinsichtlich bestimmter Leistungsspezifikationen von großer Bedeutung.
CCD, CMOS, sCMOS und BSI
Lange Zeit waren CCD-Sensoren die etablierte Technik am Markt für Fluoreszenz-Mikroskope. Das hat sich in den letzten Jahren geändert, auch wenn sie immer noch in hochwertigen Mikroskopie-Kameras verfügbar sind. Die neuere CMOS-Technologie hat sich seit vielen Jahren verbreitet und ist inzwischen auch für die besonderen Herausforderungen im wissenschaftlichen Bereich wettbewerbsfähig. Das Rauschverhalten ist nun vergleichbar oder sogar besser als bei den traditionellen CCD-Sensoren und gleichzeitig bringt die neue Technologie höhere Geschwindigkeit, höhere Auflösung und weniger Stromverbrauch/Wärmeabgabe zu niedrigeren Preisen mit sich.
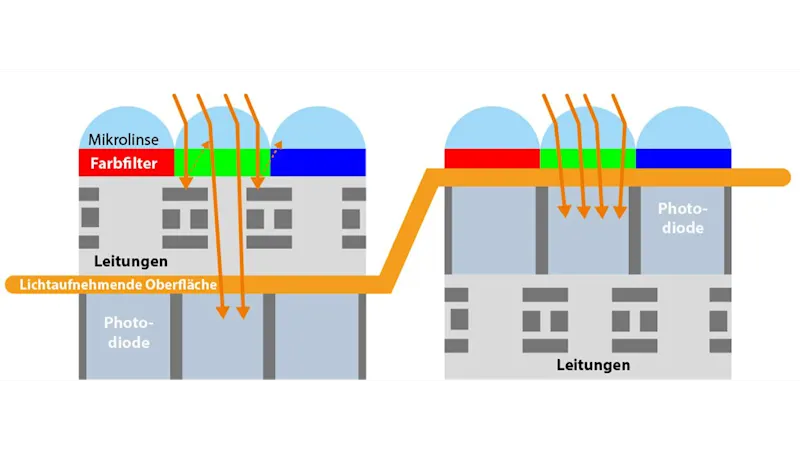
CMOS-Sensoren entwickeln sich immer noch rapide weiter. So hat eine Technologie namens Backside Illumination (BSI) ihren Weg in industrielle Bildsensoren gefunden. Diese Technologie beinhaltet eine Umkehrung der Pixelstruktur, um die lichtempfindliche Fotodiode direkt unter den Mikrolinsen zu präsentieren, was die Quanteneffizienz der Pixel erheblich steigert.
Monochrom oder Farbe
Für Fluoreszenzanwendungen werden monochrome Kameras wegen der höheren Quanteneffizienz in der Regel bevorzugt. Der technische Unterschied ist, dass bei Farbkameras Bayer-Mikrofilter auf jedem Pixel nur Licht bestimmter Wellenlängen durchlassen. Diese Filterung wird benötigt, um die Farbinformationen des Bildes mit Hilfe eines Prozesses zu berechnen, der als Debayering bezeichnet wird. Da diese Farbfilter eine bestimmte Lichtmenge blockieren, erreichen weniger Photonen den photonenreaktiven Bereich des Pixels. Zusätzlich zum Bayer-Muster auf den Sensoren stellt der IR-Sperrfilter in Farbkameras einen begrenzenden Faktor dar, da er Licht von etwa700 nm aufwärts blockiert.
Üblicherweise werden Bilder mit mehreren Fluoreszenzmarkern für die spezifische Detektion und Ko-Lokalisierung von unterschiedlichen Molekülen innerhalb eines Präparates aus separaten monochromen Bildern. Wählbare Lichtquellen und Filtersätze ermöglichen die richtige Kombination von Anregungs- und Emissionswellenlängen für jedes verwendete Fluorophor.
Bei bestimmten Anwendungen kann jedoch die Anforderung entstehen, Farbbildgebung und Fluoreszenz innerhalb eines Geräts mit nur einer Kamera durchzuführen. Dies ist möglich, wenn die Anforderungen an die Empfindlichkeit der Fluoreszenzanwendung nicht zu hoch sind.
Global und Rolling Shutter
CCD-Sensoren haben nur einen Shutter-Typ (global), während CMOS-Sensoren in zwei Ausführungen erhältlich sind: Rolling und global. Die Wahl des richtigen Sensors hat einen erheblichen Einfluss auf die Bildqualität, wenn sich die Zielobjekte bewegen. Bei Rolling-Shutter-Sensoren werden die Pixel Zeile für Zeile belichtet. Infolgedessen erzeugt ein Objekt, das seine Position zwischen der Signalerfassung von zwei Zeilen verändert hat, abweichende Bildsituationen, die eine räumliche Verzerrung im Bild erzeugen. Ein technischer Vorteil von Rolling-Shutter-Sensoren ist, dass sie weniger elektronische Teile im Pixel haben, was zu weniger Rauschen beim Auslesen führen kann. Global-Shutter-Sensoren belichten hingegen alle Pixel des Sensors gleichzeitig. In diesem Fall gibt es keine Zeitverschiebung zwischen den Belichtungen der verschiedenen Pixelzeilen und es können keine räumlichen Verzerrungen durch eine Bewegung von Objekten entstehen.
Empfindlichkeit und Dynamikbereich
Bevor die Qualität eines Bildes näher betrachtet wird, muss sichergestellt werden, dass das System empfindlich genug ist, um die Fluoreszenzsignale, die je nach Anwendung sehr schwach sein können, zu erfassen. Unter Empfindlichkeit ist die minimale Lichtmenge zu verstehen, die erforderlich ist, um ein Signal zu erzeugen, das vom Rauschen unterschieden werden kann. Ein wichtiger Wert ist die Quanteneffizienz (QE), die das Verhältnis zwischen den einfallenden Photonen der Lichtquelle und den erzeugten Elektronen des Pixels beschreibt. Sie hängt von der Wellenlänge ab, und um das beste Ergebnis zu erzielen, sollte das Spektrum eines bestimmten Sensors mit den Emissionsspektren der Fluorophore in der Anwendung übereinstimmen. Je höher die QE, desto besser ist die Ausbeute an Photonen, was kürzere Belichtungszeiten ermöglicht, das Ausbleichen der Fluorophore reduziert und die Geschwindigkeit der Bilderfassung erhöht.
Häufig ist es auch von Vorteil, eine große Bandbreite unterschiedlicher Lichtintensitäten in einer Belichtung auflösen zu können. Hier ist die Full-Well-Kapazität relevant. Sie beschreibt die maximale Anzahl von Elektronen, die von einem Pixel pro Belichtung erzeugt werden können. Je höher die Full-Well-Kapazität ist, desto mehr Licht kann eingefangen werden, bevor ein Pixel gesättigt ist, wodurch die Notwendigkeit an Sättigungsbedingten zusätzlichen Belichtungen verringert wird.
Durch die Kombination der maximalen Anzahl von Elektronen mit der niedrigsten Anzahl von Elektronen, die zur Erzeugung eines echten Signals erforderlich sind (siehe "Ausleserauschen" im nächsten Abschnitt), charakterisiert der Dynamikbereich die Gesamtfähigkeit einer Kamera, variable Lichtstärken zu erfassen und zu unterscheiden.
Schließlich gibt es noch die absolute Empfindlichkeitsschwelle, die die Anzahl der Photonen angibt, die von einem Pixel benötigt wird, um ein Signal-Rausch-Verhältnis (SNR) von 1 zu
erzeugen - was bedeutet, dass das Signal dem Rauschen entspricht. Je kleiner dieser Wert ist, desto weniger Licht wird benötigt, um ein echtes Signal zu erzeugen.
Bildqualität und Rauschen
Rauschen ist die Abweichung zwischen dem wahren Signalwert und dem Wert, der von einem Messsystem erzeugt wird. Das SNR quantifiziert das Gesamtrauschen eines bildgebenden Systems bei einem bestimmten Lichtpegel und ist ein üblicher Parameter, der zum Vergleich von Kameras verwendet wird. Je höher das SNR, desto besser die Bildqualität. Bei der Bildgebung gibt es Arten von Rauschen, die durch die Kameratechnologie nur selten - wenn überhaupt - reduziert werden können (z.B. das Photon-Shot-Noise, das durch die Eigenschaft der Photonen verursacht wird). Andere Rauscharten, die die Bildqualität beeinflussen, werden jedoch durch den Sensor selbst und die Kameratechnik erheblich beeinflusst. In den letzten Jahren wurde die etablierte CCD-Technologie in Sachen Auflösung und Bildrate zuletzt aber auch hinsichtlich der Bildqualität von modernen CMOS-Sensoren übertroffen. – so z. B. beim Ausleserauschen – auch zeitliches Dunkelrauschen – das ist das Rauschen, das einem Signal pro Belichtungsvorganghinzugefügt. Es wird in e¯/Pixel angegeben. Moderne CMOS-Sensoren erreichen ein Leserauschen von nur 2 e¯ oder sogar darunter.
Eine weitere Rauschquelle, die für Fluoreszenzanwendungen relevant ist, wird mit zunehmender Belichtungszeit wichtig; sie wird durch Dunkelstrom verursacht. Der Dunkelstrom beruht auf spontanes Auslösen von Elektronen während der Belichtung und wird in e¯/Pixel/s ausgedrückt. Als Faustregel gilt, dass sich der Dunkelstrom mit jeder Temperaturerhöhung von 7 °C verdoppelt.
Rauschtypen, die kein zeit-, sondern ein ortsbezogenes Verhalten beschreiben, werden als Fixed Pattern Noise oder Festmusterrauschen bezeichnet; dies beschreibt Abweichungen, die zwischen verschiedenen Pixeln auftreten. Es kann durch die Pixelelektronik oder auch durch über die Sensorfläche inkonsistente Temperaturen verursacht werden.
Standardisiert quantifizieren lassen sich diese Rauschtypen z. B. durch das DSNU (dark signal nonuniformity), das die Pixel-zu-Pixel-Abweichung der erzeugten Elektronen bei Dunkelheit beschreibt, und das PRNU (photoresponse nonuniformity), das Abweichung bei einem bestimmten Lichtpegel angibt. Durch das Setzen von Grenzwerten für Pixel-zu-Pixel-Abweichungen kann man diese weiter differenzieren und abweichende Pixelentsprechend als defekte Pixel klassifizieren soz. B. als Hot-Pixel die hohe Grauwerte ohne ein eigentliches Signal aufweisen. Einige Kamerahersteller korrigieren defekte Pixel bereits im Zuge der Qualitätskontrolle durch Interpolation benachbarter Pixel.
Schnittstellen
Es gibt verschiedene Schnittstellen auf dem Markt. Um zu entscheiden, welche Schnittstelle benötigt wird, sollte man je nach Anwendung folgende Punkte beachten: Daten/Bildrate, Kabellänge, Standardisierung, Integrationsaufwand und Kosten. Die Schnittstellentechnologien USB 3.0 (umbenannt in 3.2 Gen 1) und GigE stellen den aktuell üblichen Stand der Technik für die Integration in Fluoreszenzmikroskopie-basierte Systeme dar. Für beide Schnittstellen sind Vision-Standards verfügbar, die von führenden Kameraherstellern entwickelte Spezifikationen bereitstellen, um für die Kameraintegratoren das Design, den Aufwand und die Leistung von Vision-Systemen zu verbessern.
USB 3.2 Gen 1 ist die gängige und etablierte Plug-and-Play-Schnittstelle mit einfachster Integration Sie ermöglicht Datenraten von 380 MB/s also z. B. 75fps bei 5MP, was ausreichend für die meisten Anwendungen ist. Kabellängen von bis zu einigen Metern einschließlich Stromversorgung und auch die Integration von Multikameras werden unterstützt. GigE wird eingesetzt, wenn größere Kabellängen und eine präzisere Synchronisation mehrerer Kameras erforderlich sind. Die Bandbreite von GigE ist 3,8× langsamer (100 MB/s) als die genannte USB. Für beide Schnittstellen sind bereits neue Versionen mit bis zu vierfach höherer Bandbreite veröffentlicht worden, die sich jedoch im Markt erst noch etablieren müssen, wozu auch die Verfügbarmachung entsprechender Hardware-Peripherie erforderlich ist.
Kühlung
Die Temperatur des Sensors hat einen zentralen Einfluss auf den Dunkelstrom, der das SNR und die Bildqualität verschlechtert - insbesondere wenn die Lichtsignale schwach sind und längere Belichtungszeiten erforderlich werden. Die Kühlung von Kameras kann daher wichtig sein, ist aber nicht zwingend notwendig bei der Fluoreszenz-Bildgebung. Da Kühlmaßnahmen die Systemkosten erheblich beeinflussen, wird die Mehrzahl der Kameras nicht aktiv gekühlt, was für Anwendungen mit guten Fluoreszenzsignalen bereits ausreichend ist. Aber auch bei diesen Kameras hat das Design einen Einfluss auf die Sensortemperatur. Die Wärmeerzeugung sollte durch einen Betrieb mit geringer Leistungsaufnahme vermieden werden, und die Wärme sollte über das interne Hardware-Design und durch die Montage der Kamera auf einem weiteren wärmeabführenden Träger effizient nach außen transportiert werden.
Für die aktive Kühlung eines Sensors werden thermoelektrische (Peltier-)Elemente verwendet, und normalerweise führt ein integrierter Lüfter die vom Peltier-Element erzeugte Wärme nach außen ab. Der Lüfter trägt auch dazu bei, Kondensationsfeuchtigkeit bei Temperaturen unterhalb der Umgebungstemperatur zu verhindern. Wenn Vibrationen (die durch den Lüfter entstehen können) im System verhindert werden müssen, können einige Kameras sogar wassergekühlt werden.
Verbesserungen durch Firmware
Über die Hardware- und Sensorspezifikationen hinaus können die Kameras Firmware-Funktionen bieten, die die Bildqualität bei schwachen Lichtverhältnissen verbessern.
Ein Beispiel ist die Korrektur defekter Pixel. Dazu wird die Kamera während der Endkontrolle beim Hersteller bei unterschiedlichen Belichtungszeiten betrieben, und defekte Pixel im Cache der Kamera lokalisiert und gespeichert. Im Betriebsmodus werden die Werte der defekten Pixel durch die gewichtete Summe der Nachbarpixel interpoliert. Dies trägt zur Verbesserung der Bildqualität und des SNR bei.
Die aktuellen CMOS-Sensorgenerationen ermöglichen Anwendungen, die früher ohne die Investition von mehreren Tausend Euro in eine CCD-Kamera nicht möglich waren. Diese neuen Möglichkeiten werden immer wichtiger, da die Fluoreszenz in den Biowissenschaften ein zunehmend genutztes Werkzeug wird, das Strukturen und Prozesse sichtbar machen kann.
Anwendungen der Fluoreszenzmikroskopie

Die Fluoreszenz ist ein physikalisches Phänomen und nicht nur eine konkrete Technologie. Die möglichen Methoden - etwa für die Analytik, quantitative Bestimmungen oder Visualisierungen, die in den Biowissenschaften eingesetzt werden - sind nahezu unendlich. Fluorophore können an verschiedene Träger wie Proteine (oft Antikörper), Nukleinsäuren oder Mikropartikel gekoppelt werden. Sie können aber auch als gentechnische Marker in Organismen integriert werden, um zellbiologische Funktionen und Prozesse zu untersuchen. Neben den Lebenswissenschaften werden fluoreszenzbasierte Methoden auch in anderen Bereichen, wie der Materialanalyse und der Forensik, eingesetzt. Die folgenden Beispiele zeigen die vielseitigen Anwendungsmöglichkeiten der Fluoreszenz.
Bei der In-vitro-Diagnostik von Autoimmun- oder Infektionskrankheiten kann man die Technik der indirekten Immunfluoreszenz-Mikroskopie verwenden, um spezifische Antikörper im Blut des Patienten nachzuweisen.
Neben der manuellen Mikroskopie gibt es bereits automatisierte Systeme, die den Laborärzten auf der Grundlage der Fluoreszenzmuster der mit Patientenseren inkubierten Zellen einen Befundvorschlag geben. Ein anderes System wiederum analysiert Patientenseren auf Malariaerreger in weniger als 3 Minuten.

Point-of-Care-Systeme gewinnen in der medizinischen Diagnostik zunehmend an Bedeutung. Sie ermöglichen es unter anderem, durch einfache und kostengünstige Anwendungen auch in wirtschaftlich und infrastrukturell schwachen Regionen eine bessere medizinische Versorgung zu etablieren. Lab-on-a-Chip-Technologien ermöglichen die Bearbeitung von Patientenproben auf einem kleinen Chip, ohne dass eine komplexe Laborausstattung erforderlich ist.
In der Operationsmikroskopie wird der operierende Arzt zunehmend durch spezifische Fluoreszenzmarkierungen von Blutgefäßen oder Tumorgewebe unterstützt, so dass er mit Fluoreszenz-geführter Chirurgie mit perfekter Präzision operieren kann. Auch können Zahnärzte eine schnellere und spezifischere Behandlung anbieten, indem sie beispielsweise von Karies betroffene Zahnbereiche während der Behandlung selektiv sichtbar machen. Nicht zuletzt werden in der Pathologie Fluoreszenzmikroskopie-Anwendungen eingesetzt, um Gewebe aus Patientenbiopsien auf mögliche Krankheiten zu untersuchen.
Die Life-Sciences bieten ein breites Spektrum an fluoreszenzbasierten Anwendungen, bei denen mikroskopische Untersuchungen einen erheblichen Anteil haben. Die Immunfluoreszenzmikroskopie ermöglicht den spezifischen Nachweis bestimmter Proteine - zum Beispiel zum Nachweis oder zur Klärung ihrer Lokalisierung in Zellen und Geweben oder als Marker für den Beginn des Zelltods, abhängig von bestimmten Testbedingungen. Heutzutage kann die Bildgebung in lebenden Zellen auch über längere Zeiträume auf automatischen Systemen durchgeführt werden.
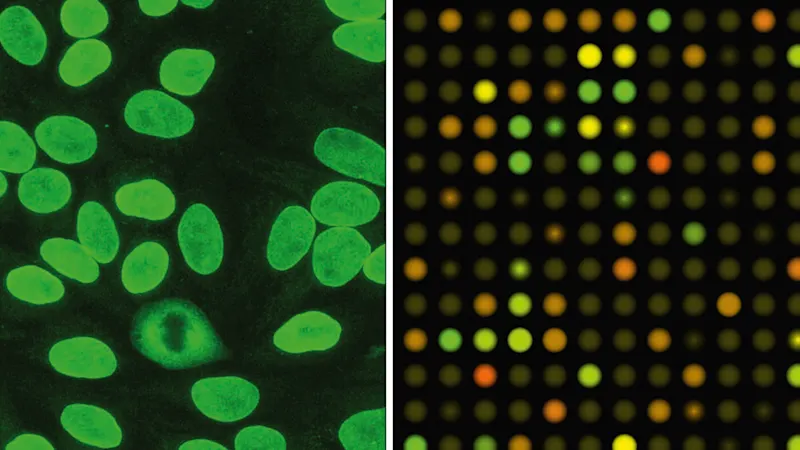
Miniaturisierung und Parallelisierung zur Erhöhung der Analysenzahlen sind in der pharmazeutischen Forschung von besonderer Bedeutung, da bei der Suche nach neuen Wirkstoffen eine sehr hohe Anzahl von Proben analytisch untersucht wird. Hier kommen Microarrays und High-Content-Screening-Systeme zum Einsatz.
Mit automatischen Koloniezählern können Fluoreszenzmarker in Petrischalen eingesetzt werden, um erfolgreich modifzierte Zellen zu selektieren und anschließend eine Probe der jeweiligen Kolonie zu entnehmen.